Tabel periodik
Tabel periodik adalah tampilan unsur-unsur kimia dalam bentuk tabel. Unsur-unsur tersebut disusun berdasarkan nomor atom (jumlah proton dalam inti atom), konfigurasi elektron, dan keberulangan sifat kimia. Tabel juga terbagi menjadi empat blok: blok -s, -p, -d, dan -f. Secara umum, dalam satu periode (baris), di sebelah kiri bersifat logam, dan di sebelah kanan bersifat non-logam.
Baris pada tabel disebut periode, sedangkan kolom disebut golongan. Enam golongan (kolom) mempunyai nama selain nomor: contoh, unsur golongan 17 adalah halogen, dan golongan 18 adalah gas mulia. Tabel periodik dapat digunakan untuk menurunkan hubungan antara sifat-sifat unsur, dan memperkirakan sifat unsur baru yang belum ditemukan atau disintesis. Tabel periodik memberikan kerangka kerja untuk melakukan analisis perilaku kimia, dan banyak digunakan dalam bidang kimia dan ilmu lainnya.
Meskipun ada para pendahulunya, tabel periodik Dmitri Mendeleev adalah yang paling dipercaya, dalam publikasinya, pada tahun 1869, sebagai tabel periodik yang pertama kali diakui secara luas. Ia mengembangkan tabelnya untuk menggambarkan tren periodik berdasarkan sifat-sifat unsur-unsur yang telah diketahui. Mendeleev juga memperkirakan beberapa sifat unsur-unsur yang belum diketahui yang akan mengisi ruang kosong dalam tabel tersebut. Sebagian besar prediksinya terbukti benar ketika unsur-unsur tersebut terungkap di kemudian hari. Tabel periodik Mendeleev telah dikembangkan dan dilengkapi dengan penemuan atau sintesis unsur-unsur baru dan pengembangan model teoretis baru untuk menjelaskan perilaku kimia.
Seluruh unsur dari nomor atom 1 (hidrogen) hingga 118 (oganesson) telah ditemukan atau disintesis, dengan penambahan terbaru (nihonium, moscovium, tennessine, dan oganesson) yang dikonfirmasi oleh International Union of Pure and Applied Chemistry (IUPAC) pada tanggal 30 Desember 2015 dan secara resmi diberi nama pada tanggal 28 November 2016: mereka menyelesaikan tujuh baris pertama Tabel periodik.[1][2] Sembilan puluh empat unsur pertama terdapat secara alami, meskipun beberapa ditemukan dalam jumlah renik dan disintesis dalam laboratorium sebelum ditemukan di alam.[n 1] Unsur-unsur mulai nomor atom 95 hingga 118 adalah unsur sintetis yang dibuat di laboratorium. Bukti menunjukkan bahwa unsur-unsur nomor 95 s/d 100 sekali ditemukan di alam, tetapi saat ini tidak dijumpai lagi.[3] Sintesis unsur dengan nomor atom yang lebih besar masih terus dikembangkan. Sejumlah radionuklida sintetis atau unsur yang berada di alam telah diproduksi di laboratorium.
Tabel periodik standar memberikan informasi dasar mengenai suatu unsur. Ada juga cara lain untuk menampilkan unsur-unsur kimia dengan memuat keterangan lebih atau dari persepektif yang berbeda.
Daftar isi
- 1Ikhtisar
- 2Metode pengelompokan
- 3Tren periodik
- 4Sejarah
- 5Tabel periodik yang berbeda
- 6Pertanyaan terbuka dan kontroversi
- 7Lihat pula
- 8Catatan kaki
- 9Referensi
- 10Daftar pustaka
- 11Pranala luar
Ikhtisar
Bentuk umum tabel periodik sebagai berikut
| [sembunyikan] | ||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Golongan | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||
| Logam alkali | Logam alkali tanah | Pniktogen | Kalkogen | Halogen | Gas Mulia | |||||||||||||||||||||||||
| Periode | ||||||||||||||||||||||||||||||
| 2 | ||||||||||||||||||||||||||||||
| 3 | ||||||||||||||||||||||||||||||
| 4 | ||||||||||||||||||||||||||||||
| 5 | ||||||||||||||||||||||||||||||
| 6 | ||||||||||||||||||||||||||||||
| 7 | ||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||
Masing-masing unsur memiliki nomor atom unik yang menunjukkan jumlah proton dalam intinya. Sebagian besar unsur memiliki jumlah netron yang berbeda untuk atom yang berbeda. Hal semacam ini dikenal sebagai isotop. Sebagai contoh, karbon memiliki tiga isotop alami: semua atom tersebut memiliki enam proton dan sebagian besarnya memiliki enam netron juga, tetapi sekitar satu persen mempunyai tujuh netron, dan sebagian renik mempunyai delapan netron. Isotop tidak disajikan terpisah dalam tabel periodik. Mereka selalu dikelompokkan bersama sebagai unsur tunggal. Massa atom unsur yang tidak memiliki isotop stabil diambil dari isotop yang paling stabil, dituliskan di dalam kurung.[4]
Beberapa presentasi memasukkan unsur nol. yaitu unsur yang tersusun hanya dari netron saja. Misalnya dalam Kimia Antariksa.
Dalam tabel periodik standar, unsur disusun menurut kenaikan nomor atom (jumlah proton dalam inti atom). Baris (periode) baru dimulai saat kulit elektron baru mempunyai elektron pertamanya. Kolom (golongan) ditentukan berdasarkan konfigurasi elektron; unsur-unsur yang memiliki kesamaan jumlah elektron dalam subkulit tertentu berada dalam kolom yang sama (contoh: oksigen dan selenium berada di kolom yang sama karena keduanya mempunyai empat elektron pada subkulit-p terluarnya). Unsur-unsur dengan kesamaan sifat kimia biasanya jatuh ke dalam golongan yang sama pada tabel periodik, meskipun dalam blok-f, dan beberapa ditemukan di blok-d, unsur-unsur dalam periode yang sama cenderung memiliki kesamaan sifat kimia. Oleh karena itu, relatif mudah untuk memperkirakan sifat kimia suatu unsur jika diketahui sifat unsur-unsur di sekelilingnya.[5]
Hingga tahun 2016, terdapat 118 unsur yang telah dikonfirmasi pada tabel periodik, meliputi unsur 1 (hidrogen) hingga 118 (oganesson), dengan penambahan terbaru (nihonium, moscovium, tennessine, dan oganesson) yang dikonfirmasi oleh International Union of Pure and Applied Chemistry (IUPAC) pada tanggal 30 Desember 2015 dan secara resmi diberi nama pada tanggal 28 November 2016: mereka menyelesaikan tujuh baris pertama Tabel periodik.[1][2]
Sebanyak 94 unsur terdapat secara alami; sisanya 20 unsur dari amerisium hingga kopernisium dan flerovium serta livermorium, hanya ada jika disintesis di laboratorium. Dari 94 unsur alami, 84 adalah primordial (unsur purba). Sepuluh lainnya muncul jika ada peluruhan dari unsur primordial.[3] Tidak ada unsur yang lebih berat daripada einsteinium (unsur 99) yang ditemui dalam jumlah besar dan bentuknya murni. Bahkan astatin (unsur 85); fransium (unsur 87) hanya terdeteksi dalam bentuk emisi cahaya dari jumlah mikroskopis (300.000 atom).[6]
Tampilan lain
| Tampilan tabel periodik | |
|---|---|
| Lantanida dan aktinida dipisah (kiri; 18 kolom) dan dimasukkan dalam tabel utama (kanan; 32 kolom) | |
Tampilan tabel periodik yang paling umum, tabel utama terdiri dari 18 kolom dan lantanida serta aktinida ditampilkan sebagai dua baris tambahan di bawah tabel utama,[7] dengan dua ruang kosong ditampilkan dalam tabel utama, yaitu di antara barium dan hafnium, dan radium dan rutherfordium. Ruang kosong ini dapat berpenanda asterik, atau deskripsi kecil unsur ("57–71"). Konvensi ini murni semata-mata format praktis. Struktur tabel yang sama dapat disajikan dalam format 32 kolom, dengan lantanida dan aktinida di dalam baris 6 dan 7 tabel utama.
Namun, berdasarkan sifat kimia dan fisika unsur-unsur, banyak struktur tabel alternatif yang telah dibuat.
Metode pengelompokan
Golongan
Golongan atau famili adalah kolom vertikal dalam tabel periodik. Golongan biasanya mempunyai tren periodik yang lebih bermakna daripada periode dan blok, yang akan dijelaskan kemudian. Teori mekanika kuantum modern dari struktur atom menjelaskan bahwa unsur-unsur yang berada dalam golongan yang sama memiliki konfigurasi elektron yang sama pada kulit valensinya.[8] Akibatnya, unsur-unsur dalam golongan yang sama cenderung memiliki sifat serta tren yang jelas seiring dengan kenaikan nomor atom.[9] Namun, dalam beberapa bagian tabel periodik, seperti blok-d dan blok-f, kesamaan horisontal lebih penting, atau lebih jelas daripada kesamaan vertikalnya.[10][11][12]
Pada konvensi tatanama internasional, golongan diberi angka numerik dari 1 hingga 18 dari kolom paling kiri (logam alkali) hingga kolom paling kanan (gas mulia).[13] Sebelumnya, dikenal penomoran menggunakan angka Romawi. Di Amerika, angka Romawi diikuti dengan huruf "A" jika golongan berada dalam blok-s atau blok-p, atau "B" jika berada pada blok-d. Angka Romawi digunakan merujuk pada angka terakhir konvensi penamaan terkini (misal: unsur golongan 4 sebelumnya adalah IVB, dan golongan 14 sebelumnya adalah golongan IVA). Di Eropa, penggunaan abjad juga sama, kecuali: "A" digunakan jika golongan berada sebelum golongan 10, dan "B" digunakan untuk golongan 10 dan seterusnya. Selain itu, golongan 8, 9, dan 10 diperlakukan sebagai satu golongan berukuran tiga, telah diketahui secara umum yang diberi tanda golongan VIII. Pada tahun 1988, digunakan sistem penamaan IUPAC baru, dan nama golongan lama telah dianggap usang.[14]
Beberapa golongan ini telah memiliki nama trivial (non-sistematis), seperti terlihat pada tabel di bawah, meskipun jarang digunakan. Golongan 3–10 tidak memiliki nama trivial dan hanya merujuk pada nomor golongannya atau nama unsur teratas dalam golongan tersebut (misalnya, "golongan skandium" untuk Golongan 3), karena hanya memiliki sedikit kesamaan tren vertikal.[13]
Unsur-unsur dalam golongan yang sama cenderung menunjukkan pola tertentu dalam hal jari-jari atom, energi ionisasi, dan elektronegativitas. Dari atas ke bawah dalam satu golongan, jari-jari atom bertambah. Oleh karena lebih banyak tingkat energi yang terisi, elektron valensi ditemukan lebih jauh dari inti atom. Dari atas ke bawah, masing-masing unsur yang berurutan memiliki energi ionisasi yang lebih rendah karena lebih mudah melepaskan elektron akibat ikatan atom yang kurang kuat. Demikian pula, dari atas ke bawah elektronegativitasnya juga semakin kecil akibat penambahan jarak antara elektron valensi dengan inti atom.[15] Terdapat perkecualian terhadap tren ini, misalnya yang terjadi pada golongan 11 di mana elektronegativitas meningkat dalam satu golongan dari atas ke bawah.[16]
| [sembunyikan]
Golongan dalam tabel periodik
| ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Nomor golongana | 1 | 2 | 3d | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||
| Mendeleev (I–VIII) | I | II | III | IV | V | VI | VII | VIII | I | II | III | IV | V | VI | VII | b | ||||
| CAS (AS, susunan A-B-A) | IA | IIA | IIIB | IVB | VB | VIB | VIIB | VIIIB | IB | IIB | IIIA | IVA | VA | VIA | VIIA | VIIIA | ||||
| IUPAC lama (Eropa, susunan A-B) | IA | IIA | IIIA | IVA | VA | VIA | VIIA | VIII | IB | IIB | IIIB | IVB | VB | VIB | VIIB | 0 | ||||
| Nama trivial | Logam alkali | Logam alkali tanah | Logam koine | Logam volatile | Ikosagene | Kristalogene | Pnictogen | Kalsogen | Halogen | Gas mulia | ||||||||||
| Nama menurut unsur | Gol. Litium | Gol. Berilium | Gol. Skandium | Gol. Titanium | Gol. Vanadium | Gol. Krom | Gol. Mangan | Gol. Besi | Gol. Kobalt | Gol. Nikel | Gol. Tembaga | Gol. Seng | Gol. Boron | Gol. Karbon | Gol. Nitrogen | Gol. Oksigen | Gol. Fluor | Gol Helium /Neon | ||
| Periode 1 | Hc | He | ||||||||||||||||||
| Periode 2 | Li | Be | B | C | N | O | F | Ne | ||||||||||||
| Periode 3 | Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||||
| Periode 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | ||
| Periode 5 | Rb | Sr | d | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |
| Periode 6 | Cs | Ba | La–Yb | Lud | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |
| Periode 7 | Fr | Ra | Ac–No | Lrd | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
| a Nomor penggolongan modern menurut IUPAC (saat ini). | ||||||||||||||||||||
| b Meskipun tidak termasuk dalam tabel asli Mendeleev, Mendeleev kemudian (1902) menerima bukti keberadaan gas mulia, dan menempatkan mereka terpisah pada "golongan 0". | ||||||||||||||||||||
| c Hidrogen (H), meskipun terdapat pada golongan 1, tetapi tidak termasuk dalam logam alkali. | ||||||||||||||||||||
| d Golongan 3: Tergantung dari sumbernya, lutetium (Lu) dan lawrensium (Lr) dapat dimasukkan; lantanum (La) dan aktinium (Ac) dapat dimasukkan; blok-f (dengan 15 lantanida dan 15 aktinida) dapat dimasukkan. | ||||||||||||||||||||
| e Nama golongan ini tidak direkomendasikan oleh IUPAC. | ||||||||||||||||||||
Periode
Periode adalah baris horizontal dalam tabel periodik. Meskipun golongan lebih menggambarkan tren periodik, tetapi ada beberapa bagian di mana tren horizontal lebih signifikan daripada tren vertikal. Seperti pada blok-f, di mana lantanida dan aktinida membentuk dua seri unsur horizontal yang substansial.[17]
Unsur-unsur dalam periode yang sama menunjukkan tren jari-jari atom, energi ionisasi, afinitas elektron, dan elektronegativitas. Dari kiri ke kanan dalam periode yang sama, jari-jari atom biasanya menyusut. Hal ini terjadi karena masing-masing unsur yang berurutan menambah proton dan elektron, yang menyebabkan elektron tertarik lebih dekat ke inti atom.[18] Penurunan jari-jari atom ini juga menyebabkan energi ionisasi meningkat dari kiri ke kanan dalam satu periode. Semakin kuat ikatan suatu unsur, semakin banyak energi yang diperlukan untuk melepas elektron. Elektronegativitas meningkat sesuai kenaikan energi ionisasi karena elektron tertarik ke inti atom.[15] Afinitas elektron juga menunjukkan kecenderungan serupa dalam periode yang sama. Logam (periode sebelah kiri) umumnya memiliki afinitas elektron yang lebih rendah daripada non logam (periode sebelah kanan), dengan pengecualian pada gas mulia.[19]
Blok
Bagian tertentu pada tabel periodik dapat dirujuk sebagai blok sesuai dengan urutan pengisian kulit elektron unsur-unsurnya. Masing-masing blok diberi nama sesuai dengan sub kulit tempat elektron terakhir berada.[20][n 2] Blok-s terdiri dari dua golongan pertama (logam alkali dan alkalil tanah) ditambah hidrogen dan helium. Blok-p terdiri dari enam golongan terakhir, yaitu golongan 13 hingga 18 sesuai IUPAC (3A hingga 8A sesuai penamaan Amerika), dan mengandung, sebagian besar, metaloid. Blok-d terdiri dari golongan 3 hingga 12 (atau golongan 3B hingga 2B dalam penggolongan sistem Amerika) dan seluruhnya merupakan logam transisi. Blok-f, seringkali diletakkan di bawah tabel utama, tidak mempunyai nomor golongan dan terdiri dari lantanida dan aktinida.[21]
Logam, metaloid, dan nonlogam
Sesuai dengan sifat fisika dan kimianya, unsur dapat diklasifikasikan ke dalam tiga kategori besar yaitu logam, metaloid dan nonlogam. Logam umumnya berkilau, padatan dengan konduktivitas tinggi, dapat membentuk aloy dengan logam lainnya dan membentuk senyawa ion serupa garam dengan nonlogam (selain gas mulia). Sebagian besar nonlogam berupa gas berwarna atau tak berwarna; nonlogam yang membentuk senyawa dengan nonlogam lainnya berikatan secara kovalen. Di antara logam dan nonlogam ada metaloid, yang mempunyai sifat di antara logam dan nonlogam atau campuran keduanya.[22]
Logam dan nonlogam dapat diklasifikasikan lebih lanjut ke dalam subkategori yang menunjukkan gradasi sifat dari logam ke nonlogam, untuk unsur-unsur dalam periode yang sama. Logam terbagi ke dalam logam alkali yang reaktif, logam alkali tanah yang kurang reaktif, lantanida dan aktinida, logam transisi, dan terakhir logam pasca-transisi dengan sifat fisika dan kimia paling lemah. Nonlogam dibagi menjadi nonlogam poliatomik, yang lebih mirip dengan metaloid; nonlogam diatomik, yang merupakan nonlogam esensial; dan gas mulia monoatomik, yang merupakan nonlogam dan hampir inert sempurna. Penggolongan terspesialisasi seperti logam refraktori dan logam mulia, yang merupakan (dalam kasus ini) logam transisi, juga diketahui[23] dan terkadang dicantumkan.[24]
Mengelompokkan unsur ke dalam kategori dan subkategori berdasarkan kesamaan sifat tidaklah sempurna. Terdapat suatu spektrum sifat di dalam masing-masing kategori dan tidaklah sulit untuk menentukan tumpangsuh pada perbatasan, seperti dalam kasus kebanyakan skema klasifikasi.[25] Berilium, misalnya, diklasifikasikan sebaga logam alkali tanah, meskipun memiliki kecenderungan amfoter secara kimia dan kebanyakan membentuk senyawa kovalen adalah dua hal yang melemahkan posisinya sebagai logam. Radon dikelompokkan sebagai nonlogam dan merupakan gas mulia tetapi mempunyai kecenderungan membentuk kation seperti logam. Dimungkinkan ada klasifikasi lainnya seperti pembagian unsur ke dalam kategori kelimpahan mineraloginya, atau struktur kristalnya. Pengkategorian unsur dimulasi sejak Hinrichs,[26] pada tahun 1869 menulis bahwa garis batas sederhana dapat digambarkan pada tabel periodik untuk menunjukkan unsur dengan kesamaan sifat, seperti logam dan nonlogam, atau unsur-unsur gas.
Tren periodik
Konfigurasi elektron
Konfigurasi elektron atau organisasi elektron yang mengorbit atom netral menunjukkan keberulangan pola atau periodisitas. Elektron menempati serangkaian kulit elektron (bernomor kulit 1, kulit 2, dst). Masing-masing kulit mengandung satu atau lebih subkulit (disebut s, p, d, f dan g). Seiring dengan naiknya nomor atom, elektron secara progresif mengisi kulit dan subkulit ini sesuai dengan aturan Madelung atau aturan orde energi, seperti ditunjukkan dalam gambar. Konfigurasi elektron neon, misalnya, adalah 1s2 2s2 2p6. Dengan nomor atom sepuluh, neon memiliki dua elektron pada kulit pertamanya, dan delapan elektron pada kulit kedua—dua pada subkulit s dan enam pada subkulit p. Dalam istilah tabel periodik, pertama kali elektron menempati kulit baru berarti memulai periode baru. Posisi ini di ditempati oleh hidrogen dan logam alkali.[27][28]
Oleh karena sifat suatu unsur sebagian besar ditentukan oleh konfigurasi elektronnya, sifat-sifat unsur menunjukkan keberulangan pola atau perilaku periodik. Contohnya seperti ditunjukkan pada gambar di bawah untuk jari-jari atom, energi ionisasi dan afinitas elektron. Ini merupakan sifat periodisitas, perwujudan dari hal yang telah dinyatakan sebelum dasar teorinya dikembangkan. Ini memicu pemapanan hukum periodik (sifat-sifat unsur berulang pada interval tertentu) dan formulasi tabel periodik pertama.[27][28]
Jari-jari atom
Jari-jari atom dalam tabel periodik bervariasi dalam cara yang dapat diperkirakan dan dijelaskan. Misalnya, jari-jari atom menurun untuk unsur-unsur yang terdapat dalam satu periode, dari logam alkali hingga gas mulia; dan jari-jari atom naik untuk unsur-unsur dalam satu golongan dari atas ke bawah. Jari-jari atom naik tajam antara gas mulia di akhir periode dan logam alkali di awal periode berikutnya. Kecenderungan jari-jari atom ini (dan berbagai sifat fisika dan kimia unsur-unsur lainnya) dapat dijelaskan menggunakan teori kulit elektron atom. Teori tersebut menyajikan bukti-bukti penting untuk pengembangan dan penegasan teori kuantum.[29]
Elektron pada subkulit-4f, mulai dari cerium (unsur 58) hingga iterbium (unsur 70), tidak terlalu efektif melindungi kenaikan muatan inti karena subkulit-4f terlalu jauh dari inti atom. Unsur-unsur tepat setelah lantanida memiliki jari-jari atom yang lebih kecil daripada yang diperkirakan dan hampir sama dengan jari-jari atom unsur-unsur tepat di atasnya.[30] Oleh karena itu, hafnium secara virtual memiliki jari-jari atom dan (sifat kimia) seperti zirkonium, dan tantalum memiliki jari-jari atom yang sama dengan niobium, dan selanjutnya. Hal ini dikenal sebagai kontraksi lantanida. Pengaruh kontraksi lantanida terpantau hingga platina (unsur 78), setelah ditutupi oleh efek relativistik yang dikenal sebagai efek pasangan inert.[31] Kontraksi blok-d, yang memiliki pengaruh sama antara blok-d dan blok-p, kurang begitu dikenal dibandingkan kontraksi lantanida, tetapi menimbulkan akibat yang serupa.[30]
Energi ionisasi
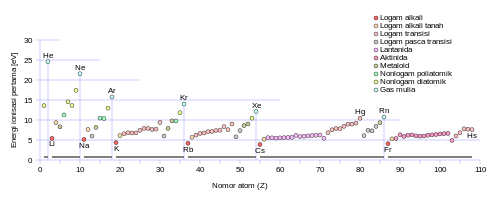
Energi ionisasi pertama adalah energi yang diserap untuk melepas satu elektron dari sebuah atom. Energi ionisasi kedua adalah energi yang diserap untuk melepas elektron kedua dari sebuah atom, dan seterusnya. Untuk sebuah atom, energi ionisasi yang berurutan meningkat sesuai dengan kenaikan derajat ionisasi. Magnesium, misalnya, memiliki energi ionisasi pertama 738 kJ/mol dan yang kedua sebesar 1.450 kj/mol. Elektron pad orbital yang lebih dekat mengalami gaya tarik elektrostatik yang lebih besar, sehingga untuk melepaskannya diperlukan energi yang lebih banyak. Energi ionisasi meningkat dari bawah ke atas (dalam satu golongan) dan dari kiri ke kanan (dalam satu periode) tabel periodik.[31]
Lonjakan besar energi ionisasi terjadi saat melepaskan satu elektron dari konfigurasi gas mulia (kulit elektron lengkap). Magnesium, misalnya, dua energi ionisasi pertama yang sudah dijelaskan di atas digunakan untuk melepaskan dua elektron 3s, dan energi ionisasi ketiga jauh lebih besar yaitu 7.730 kj/mol, untuk menghilangkan sebuah elektron 2p dari konfigurasi Mg2+yang mirip neon. Lonjakan serupa juga terjadi pada energi ionisasi atom-atom baris ketiga lainnya.[31]
Elektronegativitas
Elektronegativitas adalah kecenderungan suatu atom untuk menarik elektron.[32] Elektronegativitas suatu atom dipengaruhi oleh nomor atom dan jarak antara elektron valensi dengan inti atom. Semakin besar elektronegativitasnya, semakin kuat unsur menarik elektron. Ini pertama kali dikemukakan oleh Linus Pauling pada tahun 1932.[33] Secara umum, elektronegativitas meningkat dari kiri ke kanan dalam periode yang sama, dan menurun dari atas ke bawah dalam golongan yang sama. Oleh karena itu, fluor adalah unsur yang paling elektronegatif,[n 4] sementara sesium adalah yang paling lemah elektronegativitasnya.[16]
Terdapat beberapa pengecualian dari aturan umum ini. Galium dan germanium memiliki elektronegativitas yang lebih tinggi daripada aluminium dan silikon karena kontraksi blok-d. Unsur-unsur periode empat tepat setelah baris pertama logam transisi memiliki jari-jari atom yang lebih kecil karena elektron-3d tidak efektif melindungi kenaikan muatan inti, dan ukuran atam yang lebih kecil berkorelasi dengan elektronegativitas yang lebih tinggi.[16] Anomali elektronegativitas timbal yang lebih besar daripada talium dan bismut tampaknya lebih disebabkan pada pengumpulan data (dan ketersediaan data)—termasuk metode kalkulasi—karena metode Pauling tidak menunjukkan kejanggalan tren untuk unsur-unsur tersebut.[34]
Afinitas elektron
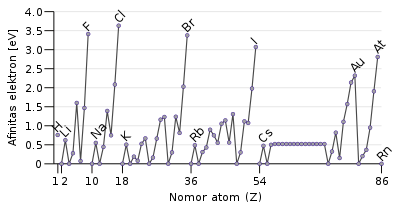
Afinitas elektron suatu atom adalah jumlah energi yang dilepaskan ketika sebuah elektron ditambahkan ke dalam atom netral untuk membentuk ion negatif. Meskipun afinitas elektron sangat bervariasi, tetapi ada pola yang dapat ditarik. Secara umum, nonlogam memiliki nilai afinitas elektron yang lebih positif daripada logam. Klorin adalah yang paling kuat dalam menarik elektron. Afinitas elektron gas mulia belum sepenuhnya terukur, oleh karenanya mungkin memiliki nilai yang sedikit negatif.[37]
Afinitas elektron umumnya meningkat sepanjang periode. Hal ini disebabkan oleh terisinya kulit valensi atom; sebuah atom golongan 17 membebaskan energi lebih besar daripada atom golongan 1 untuk menarik elektron karena atom-atom golongan 17 memiliki kulit valensi yang hampir penuh sehingga lebih stabil.[37]
Kecenderungan afinitas elektron menurun sepanjang golongan dari atas ke bawah sudah diperkirakan. Elektron tambahan akan memasuki orbital yang lebih jauh dari inti atom. Oleh karena elektron ini kurang tertarik oleh inti atom, maka pelepasan energinya juga lebih kecil ketika ditambahkan. Meski demikian, dalam satu golongan dari atas ke bawah, sekitar sepertiga unsur mengalami anomali, yaitu unsur-unsur yang lebih berat memiliki afinitas elektron yang lebih tinggi daripada unsur-unsur yang lebih ringan. Sebagian besar, hal ini akibat dari kurangnya perlindungan dari elektron-elektron d dan f. Penurunan seragan afinitas elektron hanya berlaku pada atom-atom golongan 1.[38]
Karakter logam
Semakin kecil energi ionisasi, elektronegativitas, dan afinitas elektron, semakin kuat karakter logam yang dimiliki suatu unsur. Sebaliknya, karakter nonlogam meningkat sebanding dengan peningkatan sifat-sifat di atas.[39] Sesuai dengan tren periodik ketiga sifat ini, karakter logam cenderung menurun untuk unsur-unsur dalam periode (atau baris) yang sama dan, dengan beberapa penyimpangan (sebagian besar) akibat adanya efek relativistik,[40] cenderung meningkat dari atas ke bawah untuk unsur-unsur dalam golongan (atau kolom) yang sama. Sebagian besar unsur logam (seperti sesium dan fransium) berada pada bagian kiri bawah tabel periodik tradisional dan sebagian besar unsur nonlogam (oksigen, fluor, klorin) di bagian kanan atas. Kombinasi tren horizontal dan vertikal pada karakter logam menjelaskan garis pembatas seperti anak tangga untuk memisahkan antara logam dan non logam yang dapat dijumpai pada beberapa tabel periodik. Beberapa praktisi mengelompokkan unsur-unsur yang ada di sekitar garis batas tersebut sebagai metaloid.[41][42]
Tabel periodik
Tabel periodik adalah tampilan unsur-unsur kimia dalam bentuk tabel. Unsur-unsur tersebut disusun berdasarkan nomor atom (jumlah proton dalam inti atom), konfigurasi elektron, dan keberulangan sifat kimia. Tabel juga terbagi menjadi empat blok: blok -s, -p, -d, dan -f. Secara umum, dalam satu periode (baris), di sebelah kiri bersifat logam, dan di sebelah kanan bersifat non-logam.
Baris pada tabel disebut periode, sedangkan kolom disebut golongan. Enam golongan (kolom) mempunyai nama selain nomor: contoh, unsur golongan 17 adalah halogen, dan golongan 18 adalah gas mulia. Tabel periodik dapat digunakan untuk menurunkan hubungan antara sifat-sifat unsur, dan memperkirakan sifat unsur baru yang belum ditemukan atau disintesis. Tabel periodik memberikan kerangka kerja untuk melakukan analisis perilaku kimia, dan banyak digunakan dalam bidang kimia dan ilmu lainnya.
Meskipun ada para pendahulunya, tabel periodik Dmitri Mendeleev adalah yang paling dipercaya, dalam publikasinya, pada tahun 1869, sebagai tabel periodik yang pertama kali diakui secara luas. Ia mengembangkan tabelnya untuk menggambarkan tren periodik berdasarkan sifat-sifat unsur-unsur yang telah diketahui. Mendeleev juga memperkirakan beberapa sifat unsur-unsur yang belum diketahui yang akan mengisi ruang kosong dalam tabel tersebut. Sebagian besar prediksinya terbukti benar ketika unsur-unsur tersebut terungkap di kemudian hari. Tabel periodik Mendeleev telah dikembangkan dan dilengkapi dengan penemuan atau sintesis unsur-unsur baru dan pengembangan model teoretis baru untuk menjelaskan perilaku kimia.
Seluruh unsur dari nomor atom 1 (hidrogen) hingga 118 (oganesson) telah ditemukan atau disintesis, dengan penambahan terbaru (nihonium, moscovium, tennessine, dan oganesson) yang dikonfirmasi oleh International Union of Pure and Applied Chemistry (IUPAC) pada tanggal 30 Desember 2015 dan secara resmi diberi nama pada tanggal 28 November 2016: mereka menyelesaikan tujuh baris pertama Tabel periodik.[1][2] Sembilan puluh empat unsur pertama terdapat secara alami, meskipun beberapa ditemukan dalam jumlah renik dan disintesis dalam laboratorium sebelum ditemukan di alam.[n 1] Unsur-unsur mulai nomor atom 95 hingga 118 adalah unsur sintetis yang dibuat di laboratorium. Bukti menunjukkan bahwa unsur-unsur nomor 95 s/d 100 sekali ditemukan di alam, tetapi saat ini tidak dijumpai lagi.[3] Sintesis unsur dengan nomor atom yang lebih besar masih terus dikembangkan. Sejumlah radionuklida sintetis atau unsur yang berada di alam telah diproduksi di laboratorium.
Tabel periodik standar memberikan informasi dasar mengenai suatu unsur. Ada juga cara lain untuk menampilkan unsur-unsur kimia dengan memuat keterangan lebih atau dari persepektif yang berbeda.
Daftar isi
- 1Ikhtisar
- 2Metode pengelompokan
- 3Tren periodik
- 4Sejarah
- 5Tabel periodik yang berbeda
- 6Pertanyaan terbuka dan kontroversi
- 7Lihat pula
- 8Catatan kaki
- 9Referensi
- 10Daftar pustaka
- 11Pranala luar
Ikhtisar
Bentuk umum tabel periodik sebagai berikut
| [sembunyikan] | ||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Golongan | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||
| Logam alkali | Logam alkali tanah | Pniktogen | Kalkogen | Halogen | Gas Mulia | |||||||||||||||||||||||||
| Periode | ||||||||||||||||||||||||||||||
| 2 | ||||||||||||||||||||||||||||||
| 3 | ||||||||||||||||||||||||||||||
| 4 | ||||||||||||||||||||||||||||||
| 5 | ||||||||||||||||||||||||||||||
| 6 | ||||||||||||||||||||||||||||||
| 7 | ||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||
Masing-masing unsur memiliki nomor atom unik yang menunjukkan jumlah proton dalam intinya. Sebagian besar unsur memiliki jumlah netron yang berbeda untuk atom yang berbeda. Hal semacam ini dikenal sebagai isotop. Sebagai contoh, karbon memiliki tiga isotop alami: semua atom tersebut memiliki enam proton dan sebagian besarnya memiliki enam netron juga, tetapi sekitar satu persen mempunyai tujuh netron, dan sebagian renik mempunyai delapan netron. Isotop tidak disajikan terpisah dalam tabel periodik. Mereka selalu dikelompokkan bersama sebagai unsur tunggal. Massa atom unsur yang tidak memiliki isotop stabil diambil dari isotop yang paling stabil, dituliskan di dalam kurung.[4]
Beberapa presentasi memasukkan unsur nol. yaitu unsur yang tersusun hanya dari netron saja. Misalnya dalam Kimia Antariksa.
Dalam tabel periodik standar, unsur disusun menurut kenaikan nomor atom (jumlah proton dalam inti atom). Baris (periode) baru dimulai saat kulit elektron baru mempunyai elektron pertamanya. Kolom (golongan) ditentukan berdasarkan konfigurasi elektron; unsur-unsur yang memiliki kesamaan jumlah elektron dalam subkulit tertentu berada dalam kolom yang sama (contoh: oksigen dan selenium berada di kolom yang sama karena keduanya mempunyai empat elektron pada subkulit-p terluarnya). Unsur-unsur dengan kesamaan sifat kimia biasanya jatuh ke dalam golongan yang sama pada tabel periodik, meskipun dalam blok-f, dan beberapa ditemukan di blok-d, unsur-unsur dalam periode yang sama cenderung memiliki kesamaan sifat kimia. Oleh karena itu, relatif mudah untuk memperkirakan sifat kimia suatu unsur jika diketahui sifat unsur-unsur di sekelilingnya.[5]
Hingga tahun 2016, terdapat 118 unsur yang telah dikonfirmasi pada tabel periodik, meliputi unsur 1 (hidrogen) hingga 118 (oganesson), dengan penambahan terbaru (nihonium, moscovium, tennessine, dan oganesson) yang dikonfirmasi oleh International Union of Pure and Applied Chemistry (IUPAC) pada tanggal 30 Desember 2015 dan secara resmi diberi nama pada tanggal 28 November 2016: mereka menyelesaikan tujuh baris pertama Tabel periodik.[1][2]
Sebanyak 94 unsur terdapat secara alami; sisanya 20 unsur dari amerisium hingga kopernisium dan flerovium serta livermorium, hanya ada jika disintesis di laboratorium. Dari 94 unsur alami, 84 adalah primordial (unsur purba). Sepuluh lainnya muncul jika ada peluruhan dari unsur primordial.[3] Tidak ada unsur yang lebih berat daripada einsteinium (unsur 99) yang ditemui dalam jumlah besar dan bentuknya murni. Bahkan astatin (unsur 85); fransium (unsur 87) hanya terdeteksi dalam bentuk emisi cahaya dari jumlah mikroskopis (300.000 atom).[6]
Tampilan lain
| Tampilan tabel periodik | |
|---|---|
| Lantanida dan aktinida dipisah (kiri; 18 kolom) dan dimasukkan dalam tabel utama (kanan; 32 kolom) | |
Tampilan tabel periodik yang paling umum, tabel utama terdiri dari 18 kolom dan lantanida serta aktinida ditampilkan sebagai dua baris tambahan di bawah tabel utama,[7] dengan dua ruang kosong ditampilkan dalam tabel utama, yaitu di antara barium dan hafnium, dan radium dan rutherfordium. Ruang kosong ini dapat berpenanda asterik, atau deskripsi kecil unsur ("57–71"). Konvensi ini murni semata-mata format praktis. Struktur tabel yang sama dapat disajikan dalam format 32 kolom, dengan lantanida dan aktinida di dalam baris 6 dan 7 tabel utama.
Namun, berdasarkan sifat kimia dan fisika unsur-unsur, banyak struktur tabel alternatif yang telah dibuat.
Metode pengelompokan
Golongan
Golongan atau famili adalah kolom vertikal dalam tabel periodik. Golongan biasanya mempunyai tren periodik yang lebih bermakna daripada periode dan blok, yang akan dijelaskan kemudian. Teori mekanika kuantum modern dari struktur atom menjelaskan bahwa unsur-unsur yang berada dalam golongan yang sama memiliki konfigurasi elektron yang sama pada kulit valensinya.[8] Akibatnya, unsur-unsur dalam golongan yang sama cenderung memiliki sifat serta tren yang jelas seiring dengan kenaikan nomor atom.[9] Namun, dalam beberapa bagian tabel periodik, seperti blok-d dan blok-f, kesamaan horisontal lebih penting, atau lebih jelas daripada kesamaan vertikalnya.[10][11][12]
Pada konvensi tatanama internasional, golongan diberi angka numerik dari 1 hingga 18 dari kolom paling kiri (logam alkali) hingga kolom paling kanan (gas mulia).[13] Sebelumnya, dikenal penomoran menggunakan angka Romawi. Di Amerika, angka Romawi diikuti dengan huruf "A" jika golongan berada dalam blok-s atau blok-p, atau "B" jika berada pada blok-d. Angka Romawi digunakan merujuk pada angka terakhir konvensi penamaan terkini (misal: unsur golongan 4 sebelumnya adalah IVB, dan golongan 14 sebelumnya adalah golongan IVA). Di Eropa, penggunaan abjad juga sama, kecuali: "A" digunakan jika golongan berada sebelum golongan 10, dan "B" digunakan untuk golongan 10 dan seterusnya. Selain itu, golongan 8, 9, dan 10 diperlakukan sebagai satu golongan berukuran tiga, telah diketahui secara umum yang diberi tanda golongan VIII. Pada tahun 1988, digunakan sistem penamaan IUPAC baru, dan nama golongan lama telah dianggap usang.[14]
Beberapa golongan ini telah memiliki nama trivial (non-sistematis), seperti terlihat pada tabel di bawah, meskipun jarang digunakan. Golongan 3–10 tidak memiliki nama trivial dan hanya merujuk pada nomor golongannya atau nama unsur teratas dalam golongan tersebut (misalnya, "golongan skandium" untuk Golongan 3), karena hanya memiliki sedikit kesamaan tren vertikal.[13]
Unsur-unsur dalam golongan yang sama cenderung menunjukkan pola tertentu dalam hal jari-jari atom, energi ionisasi, dan elektronegativitas. Dari atas ke bawah dalam satu golongan, jari-jari atom bertambah. Oleh karena lebih banyak tingkat energi yang terisi, elektron valensi ditemukan lebih jauh dari inti atom. Dari atas ke bawah, masing-masing unsur yang berurutan memiliki energi ionisasi yang lebih rendah karena lebih mudah melepaskan elektron akibat ikatan atom yang kurang kuat. Demikian pula, dari atas ke bawah elektronegativitasnya juga semakin kecil akibat penambahan jarak antara elektron valensi dengan inti atom.[15] Terdapat perkecualian terhadap tren ini, misalnya yang terjadi pada golongan 11 di mana elektronegativitas meningkat dalam satu golongan dari atas ke bawah.[16]
| [sembunyikan]
Golongan dalam tabel periodik
| ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Nomor golongana | 1 | 2 | 3d | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||
| Mendeleev (I–VIII) | I | II | III | IV | V | VI | VII | VIII | I | II | III | IV | V | VI | VII | b | ||||
| CAS (AS, susunan A-B-A) | IA | IIA | IIIB | IVB | VB | VIB | VIIB | VIIIB | IB | IIB | IIIA | IVA | VA | VIA | VIIA | VIIIA | ||||
| IUPAC lama (Eropa, susunan A-B) | IA | IIA | IIIA | IVA | VA | VIA | VIIA | VIII | IB | IIB | IIIB | IVB | VB | VIB | VIIB | 0 | ||||
| Nama trivial | Logam alkali | Logam alkali tanah | Logam koine | Logam volatile | Ikosagene | Kristalogene | Pnictogen | Kalsogen | Halogen | Gas mulia | ||||||||||
| Nama menurut unsur | Gol. Litium | Gol. Berilium | Gol. Skandium | Gol. Titanium | Gol. Vanadium | Gol. Krom | Gol. Mangan | Gol. Besi | Gol. Kobalt | Gol. Nikel | Gol. Tembaga | Gol. Seng | Gol. Boron | Gol. Karbon | Gol. Nitrogen | Gol. Oksigen | Gol. Fluor | Gol Helium /Neon | ||
| Periode 1 | Hc | He | ||||||||||||||||||
| Periode 2 | Li | Be | B | C | N | O | F | Ne | ||||||||||||
| Periode 3 | Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||||
| Periode 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | ||
| Periode 5 | Rb | Sr | d | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |
| Periode 6 | Cs | Ba | La–Yb | Lud | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |
| Periode 7 | Fr | Ra | Ac–No | Lrd | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
| a Nomor penggolongan modern menurut IUPAC (saat ini). | ||||||||||||||||||||
| b Meskipun tidak termasuk dalam tabel asli Mendeleev, Mendeleev kemudian (1902) menerima bukti keberadaan gas mulia, dan menempatkan mereka terpisah pada "golongan 0". | ||||||||||||||||||||
| c Hidrogen (H), meskipun terdapat pada golongan 1, tetapi tidak termasuk dalam logam alkali. | ||||||||||||||||||||
| d Golongan 3: Tergantung dari sumbernya, lutetium (Lu) dan lawrensium (Lr) dapat dimasukkan; lantanum (La) dan aktinium (Ac) dapat dimasukkan; blok-f (dengan 15 lantanida dan 15 aktinida) dapat dimasukkan. | ||||||||||||||||||||
| e Nama golongan ini tidak direkomendasikan oleh IUPAC. | ||||||||||||||||||||
Periode
Periode adalah baris horizontal dalam tabel periodik. Meskipun golongan lebih menggambarkan tren periodik, tetapi ada beberapa bagian di mana tren horizontal lebih signifikan daripada tren vertikal. Seperti pada blok-f, di mana lantanida dan aktinida membentuk dua seri unsur horizontal yang substansial.[17]
Unsur-unsur dalam periode yang sama menunjukkan tren jari-jari atom, energi ionisasi, afinitas elektron, dan elektronegativitas. Dari kiri ke kanan dalam periode yang sama, jari-jari atom biasanya menyusut. Hal ini terjadi karena masing-masing unsur yang berurutan menambah proton dan elektron, yang menyebabkan elektron tertarik lebih dekat ke inti atom.[18] Penurunan jari-jari atom ini juga menyebabkan energi ionisasi meningkat dari kiri ke kanan dalam satu periode. Semakin kuat ikatan suatu unsur, semakin banyak energi yang diperlukan untuk melepas elektron. Elektronegativitas meningkat sesuai kenaikan energi ionisasi karena elektron tertarik ke inti atom.[15] Afinitas elektron juga menunjukkan kecenderungan serupa dalam periode yang sama. Logam (periode sebelah kiri) umumnya memiliki afinitas elektron yang lebih rendah daripada non logam (periode sebelah kanan), dengan pengecualian pada gas mulia.[19]
Blok
Bagian tertentu pada tabel periodik dapat dirujuk sebagai blok sesuai dengan urutan pengisian kulit elektron unsur-unsurnya. Masing-masing blok diberi nama sesuai dengan sub kulit tempat elektron terakhir berada.[20][n 2] Blok-s terdiri dari dua golongan pertama (logam alkali dan alkalil tanah) ditambah hidrogen dan helium. Blok-p terdiri dari enam golongan terakhir, yaitu golongan 13 hingga 18 sesuai IUPAC (3A hingga 8A sesuai penamaan Amerika), dan mengandung, sebagian besar, metaloid. Blok-d terdiri dari golongan 3 hingga 12 (atau golongan 3B hingga 2B dalam penggolongan sistem Amerika) dan seluruhnya merupakan logam transisi. Blok-f, seringkali diletakkan di bawah tabel utama, tidak mempunyai nomor golongan dan terdiri dari lantanida dan aktinida.[21]
Logam, metaloid, dan nonlogam
Sesuai dengan sifat fisika dan kimianya, unsur dapat diklasifikasikan ke dalam tiga kategori besar yaitu logam, metaloid dan nonlogam. Logam umumnya berkilau, padatan dengan konduktivitas tinggi, dapat membentuk aloy dengan logam lainnya dan membentuk senyawa ion serupa garam dengan nonlogam (selain gas mulia). Sebagian besar nonlogam berupa gas berwarna atau tak berwarna; nonlogam yang membentuk senyawa dengan nonlogam lainnya berikatan secara kovalen. Di antara logam dan nonlogam ada metaloid, yang mempunyai sifat di antara logam dan nonlogam atau campuran keduanya.[22]
Logam dan nonlogam dapat diklasifikasikan lebih lanjut ke dalam subkategori yang menunjukkan gradasi sifat dari logam ke nonlogam, untuk unsur-unsur dalam periode yang sama. Logam terbagi ke dalam logam alkali yang reaktif, logam alkali tanah yang kurang reaktif, lantanida dan aktinida, logam transisi, dan terakhir logam pasca-transisi dengan sifat fisika dan kimia paling lemah. Nonlogam dibagi menjadi nonlogam poliatomik, yang lebih mirip dengan metaloid; nonlogam diatomik, yang merupakan nonlogam esensial; dan gas mulia monoatomik, yang merupakan nonlogam dan hampir inert sempurna. Penggolongan terspesialisasi seperti logam refraktori dan logam mulia, yang merupakan (dalam kasus ini) logam transisi, juga diketahui[23] dan terkadang dicantumkan.[24]
Mengelompokkan unsur ke dalam kategori dan subkategori berdasarkan kesamaan sifat tidaklah sempurna. Terdapat suatu spektrum sifat di dalam masing-masing kategori dan tidaklah sulit untuk menentukan tumpangsuh pada perbatasan, seperti dalam kasus kebanyakan skema klasifikasi.[25] Berilium, misalnya, diklasifikasikan sebaga logam alkali tanah, meskipun memiliki kecenderungan amfoter secara kimia dan kebanyakan membentuk senyawa kovalen adalah dua hal yang melemahkan posisinya sebagai logam. Radon dikelompokkan sebagai nonlogam dan merupakan gas mulia tetapi mempunyai kecenderungan membentuk kation seperti logam. Dimungkinkan ada klasifikasi lainnya seperti pembagian unsur ke dalam kategori kelimpahan mineraloginya, atau struktur kristalnya. Pengkategorian unsur dimulasi sejak Hinrichs,[26] pada tahun 1869 menulis bahwa garis batas sederhana dapat digambarkan pada tabel periodik untuk menunjukkan unsur dengan kesamaan sifat, seperti logam dan nonlogam, atau unsur-unsur gas.
Tren periodik
Konfigurasi elektron
Konfigurasi elektron atau organisasi elektron yang mengorbit atom netral menunjukkan keberulangan pola atau periodisitas. Elektron menempati serangkaian kulit elektron (bernomor kulit 1, kulit 2, dst). Masing-masing kulit mengandung satu atau lebih subkulit (disebut s, p, d, f dan g). Seiring dengan naiknya nomor atom, elektron secara progresif mengisi kulit dan subkulit ini sesuai dengan aturan Madelung atau aturan orde energi, seperti ditunjukkan dalam gambar. Konfigurasi elektron neon, misalnya, adalah 1s2 2s2 2p6. Dengan nomor atom sepuluh, neon memiliki dua elektron pada kulit pertamanya, dan delapan elektron pada kulit kedua—dua pada subkulit s dan enam pada subkulit p. Dalam istilah tabel periodik, pertama kali elektron menempati kulit baru berarti memulai periode baru. Posisi ini di ditempati oleh hidrogen dan logam alkali.[27][28]
Oleh karena sifat suatu unsur sebagian besar ditentukan oleh konfigurasi elektronnya, sifat-sifat unsur menunjukkan keberulangan pola atau perilaku periodik. Contohnya seperti ditunjukkan pada gambar di bawah untuk jari-jari atom, energi ionisasi dan afinitas elektron. Ini merupakan sifat periodisitas, perwujudan dari hal yang telah dinyatakan sebelum dasar teorinya dikembangkan. Ini memicu pemapanan hukum periodik (sifat-sifat unsur berulang pada interval tertentu) dan formulasi tabel periodik pertama.[27][28]
Jari-jari atom
Jari-jari atom dalam tabel periodik bervariasi dalam cara yang dapat diperkirakan dan dijelaskan. Misalnya, jari-jari atom menurun untuk unsur-unsur yang terdapat dalam satu periode, dari logam alkali hingga gas mulia; dan jari-jari atom naik untuk unsur-unsur dalam satu golongan dari atas ke bawah. Jari-jari atom naik tajam antara gas mulia di akhir periode dan logam alkali di awal periode berikutnya. Kecenderungan jari-jari atom ini (dan berbagai sifat fisika dan kimia unsur-unsur lainnya) dapat dijelaskan menggunakan teori kulit elektron atom. Teori tersebut menyajikan bukti-bukti penting untuk pengembangan dan penegasan teori kuantum.[29]
Elektron pada subkulit-4f, mulai dari cerium (unsur 58) hingga iterbium (unsur 70), tidak terlalu efektif melindungi kenaikan muatan inti karena subkulit-4f terlalu jauh dari inti atom. Unsur-unsur tepat setelah lantanida memiliki jari-jari atom yang lebih kecil daripada yang diperkirakan dan hampir sama dengan jari-jari atom unsur-unsur tepat di atasnya.[30] Oleh karena itu, hafnium secara virtual memiliki jari-jari atom dan (sifat kimia) seperti zirkonium, dan tantalum memiliki jari-jari atom yang sama dengan niobium, dan selanjutnya. Hal ini dikenal sebagai kontraksi lantanida. Pengaruh kontraksi lantanida terpantau hingga platina (unsur 78), setelah ditutupi oleh efek relativistik yang dikenal sebagai efek pasangan inert.[31] Kontraksi blok-d, yang memiliki pengaruh sama antara blok-d dan blok-p, kurang begitu dikenal dibandingkan kontraksi lantanida, tetapi menimbulkan akibat yang serupa.[30]
Energi ionisasi
Energi ionisasi pertama adalah energi yang diserap untuk melepas satu elektron dari sebuah atom. Energi ionisasi kedua adalah energi yang diserap untuk melepas elektron kedua dari sebuah atom, dan seterusnya. Untuk sebuah atom, energi ionisasi yang berurutan meningkat sesuai dengan kenaikan derajat ionisasi. Magnesium, misalnya, memiliki energi ionisasi pertama 738 kJ/mol dan yang kedua sebesar 1.450 kj/mol. Elektron pad orbital yang lebih dekat mengalami gaya tarik elektrostatik yang lebih besar, sehingga untuk melepaskannya diperlukan energi yang lebih banyak. Energi ionisasi meningkat dari bawah ke atas (dalam satu golongan) dan dari kiri ke kanan (dalam satu periode) tabel periodik.[31]
Lonjakan besar energi ionisasi terjadi saat melepaskan satu elektron dari konfigurasi gas mulia (kulit elektron lengkap). Magnesium, misalnya, dua energi ionisasi pertama yang sudah dijelaskan di atas digunakan untuk melepaskan dua elektron 3s, dan energi ionisasi ketiga jauh lebih besar yaitu 7.730 kj/mol, untuk menghilangkan sebuah elektron 2p dari konfigurasi Mg2+yang mirip neon. Lonjakan serupa juga terjadi pada energi ionisasi atom-atom baris ketiga lainnya.[31]
Elektronegativitas
Elektronegativitas adalah kecenderungan suatu atom untuk menarik elektron.[32] Elektronegativitas suatu atom dipengaruhi oleh nomor atom dan jarak antara elektron valensi dengan inti atom. Semakin besar elektronegativitasnya, semakin kuat unsur menarik elektron. Ini pertama kali dikemukakan oleh Linus Pauling pada tahun 1932.[33] Secara umum, elektronegativitas meningkat dari kiri ke kanan dalam periode yang sama, dan menurun dari atas ke bawah dalam golongan yang sama. Oleh karena itu, fluor adalah unsur yang paling elektronegatif,[n 4] sementara sesium adalah yang paling lemah elektronegativitasnya.[16]
Terdapat beberapa pengecualian dari aturan umum ini. Galium dan germanium memiliki elektronegativitas yang lebih tinggi daripada aluminium dan silikon karena kontraksi blok-d. Unsur-unsur periode empat tepat setelah baris pertama logam transisi memiliki jari-jari atom yang lebih kecil karena elektron-3d tidak efektif melindungi kenaikan muatan inti, dan ukuran atam yang lebih kecil berkorelasi dengan elektronegativitas yang lebih tinggi.[16] Anomali elektronegativitas timbal yang lebih besar daripada talium dan bismut tampaknya lebih disebabkan pada pengumpulan data (dan ketersediaan data)—termasuk metode kalkulasi—karena metode Pauling tidak menunjukkan kejanggalan tren untuk unsur-unsur tersebut.[34]
Afinitas elektron
Afinitas elektron suatu atom adalah jumlah energi yang dilepaskan ketika sebuah elektron ditambahkan ke dalam atom netral untuk membentuk ion negatif. Meskipun afinitas elektron sangat bervariasi, tetapi ada pola yang dapat ditarik. Secara umum, nonlogam memiliki nilai afinitas elektron yang lebih positif daripada logam. Klorin adalah yang paling kuat dalam menarik elektron. Afinitas elektron gas mulia belum sepenuhnya terukur, oleh karenanya mungkin memiliki nilai yang sedikit negatif.[37]
Afinitas elektron umumnya meningkat sepanjang periode. Hal ini disebabkan oleh terisinya kulit valensi atom; sebuah atom golongan 17 membebaskan energi lebih besar daripada atom golongan 1 untuk menarik elektron karena atom-atom golongan 17 memiliki kulit valensi yang hampir penuh sehingga lebih stabil.[37]
Kecenderungan afinitas elektron menurun sepanjang golongan dari atas ke bawah sudah diperkirakan. Elektron tambahan akan memasuki orbital yang lebih jauh dari inti atom. Oleh karena elektron ini kurang tertarik oleh inti atom, maka pelepasan energinya juga lebih kecil ketika ditambahkan. Meski demikian, dalam satu golongan dari atas ke bawah, sekitar sepertiga unsur mengalami anomali, yaitu unsur-unsur yang lebih berat memiliki afinitas elektron yang lebih tinggi daripada unsur-unsur yang lebih ringan. Sebagian besar, hal ini akibat dari kurangnya perlindungan dari elektron-elektron d dan f. Penurunan seragan afinitas elektron hanya berlaku pada atom-atom golongan 1.[38]
Karakter logam
Semakin kecil energi ionisasi, elektronegativitas, dan afinitas elektron, semakin kuat karakter logam yang dimiliki suatu unsur. Sebaliknya, karakter nonlogam meningkat sebanding dengan peningkatan sifat-sifat di atas.[39] Sesuai dengan tren periodik ketiga sifat ini, karakter logam cenderung menurun untuk unsur-unsur dalam periode (atau baris) yang sama dan, dengan beberapa penyimpangan (sebagian besar) akibat adanya efek relativistik,[40] cenderung meningkat dari atas ke bawah untuk unsur-unsur dalam golongan (atau kolom) yang sama. Sebagian besar unsur logam (seperti sesium dan fransium) berada pada bagian kiri bawah tabel periodik tradisional dan sebagian besar unsur nonlogam (oksigen, fluor, klorin) di bagian kanan atas. Kombinasi tren horizontal dan vertikal pada karakter logam menjelaskan garis pembatas seperti anak tangga untuk memisahkan antara logam dan non logam yang dapat dijumpai pada beberapa tabel periodik. Beberapa praktisi mengelompokkan unsur-unsur yang ada di sekitar garis batas tersebut sebagai metaloid.[41][42]













No comments:
Post a Comment